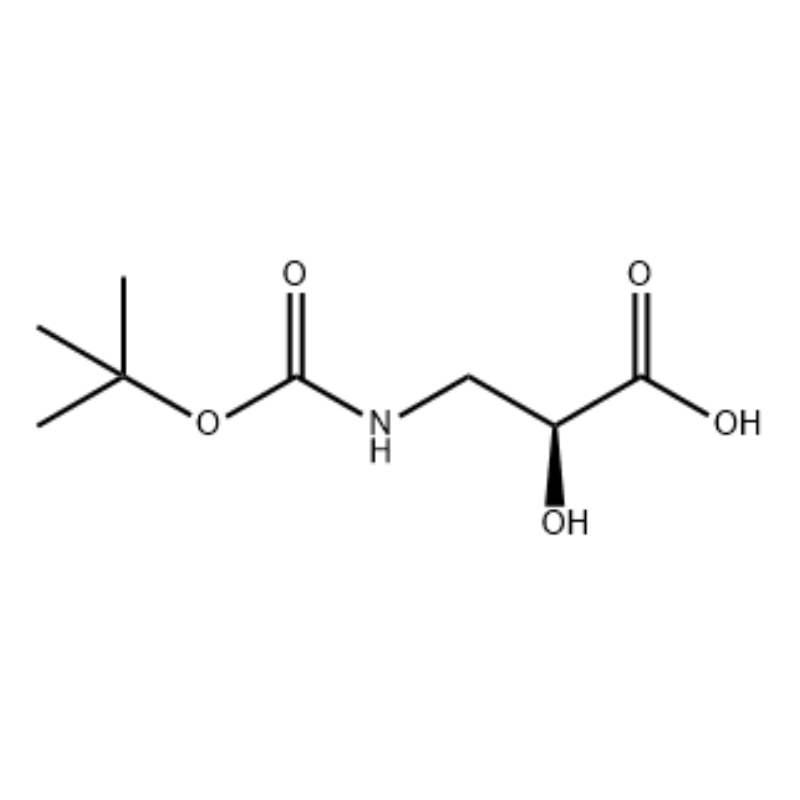
(S)-izoserina 15a (21 g, 0,20 mol) a fost dizolvată în tetrahidrofuran (100 mL) și un amestec de solvent de soluție apoasă de hidroxid de sodiu 10% (100 mL), dicarbonat de di-tert-butil (50 mL, 0,22 mol) a fost Reacția a fost efectuată la temperatura camerei timp de 9 ore. Faza apoasă a fost ajustată la pH 2 cu acid clorhidric 4 mol/L și extrasă cu diclormetan/metanol (v/v = 5/1, 50 mL × 3). ) şi uscat pe sulfat de sodiu anhidru.Se filtrează prin aspiraţie, se concentrează sub presiune redusă.Compusul din titlu 15b a fost obţinut ca un ulei incolor (35 g, randament: 85%).
La o soluție sub agitare de S-izoserină (4,0 g, 0,038 mol) în dioxan: H2O (100 mL, 1:1 v/v) la 0°C s-a adăugat N-metilmorfolină (4,77 mL, 0,043 mol), urmată de BoC2O (11,28 mL, 0,049 mol) şi reacţia a fost agitată peste noapte cu încălzire treptată la temperatura camerei.S-a adăugat apoi glicină (1,0 g, 0,013 mol) şi reacţia a fost agitată timp de 20 min.Reacţia a fost răcită la 0°C şi soluţie apoasă saturată.Sa adăugat NaHC03 (75 ml).Stratul apos a fost spălat cu acetat de etil (2 x 60 mL) şi apoi acidulat la pH 1 cu NaHS04.Această soluție a fost apoi extrasă cu acetat de etil (3 x 70 ml) și aceste straturi organice combinate au fost uscate pe Na2S04, filtrate și concentrate la sec pentru a da acidul N-Boc-3-ammo-2(S)-hidroxi-propanoic dorit. (6,30 g, 0,031 mmol, randament 81,5 procente): 1H RMN (400 MHz, CDC13) 5 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m) , 2 H), 2,09 (s, 1 H), 1,42 (s, 9 H);13C RMN (IOO MHz, CDC13) 5 174,72, 158,17, 82, 71,85, 44,28, 28,45.
acid N-Boc-3-amino-2(S)-hidroxi-propionic;La o soluție sub agitare de S-izoserină (4,0 g, 0,038 mol) în dioxan: H2O (100 mL, 1:1 v/v) la 0°C s-a adăugat N-metilmorfolină (4,77 mL, 0,043 mol), urmată de BoC2O (11,28 mL, 0,049 mol) şi reacţia a fost agitată peste noapte cu încălzire treptată la temperatura camerei.S-a adăugat apoi glicină (1,0 g, 0,013 mol) şi reacţia a fost agitată timp de 20 min.Reacţia a fost răcită la 0°C şi sat.Sa adăugat NaHC03 (75 ml).Stratul apos a fost spălat cu acetat de etil (2 x 60 mL) şi apoi acidulat la pH 1 cu NaHS04.Această soluție a fost apoi extrasă cu acetat de etil (3 x 70 ml) și aceste straturi organice combinate au fost uscate pe Na2S04, filtrate și concentrate la sec pentru a da acidul N-Boc-3-amino-2(5)-hidroxi-propanoic dorit. (6,30 g, 0,031 mmol, randament 81,5 procente): 1H RMN (400 MHz, CDC13) 5 7,45 (bs, 1 H), 5,28 (bs, 1 H), 4,26 (m, 1 H), 3,40-3,62 (m) , 2 H), 2,09 (s, 1 H), 1,42 (s, 9 H);13C RMN (100 MHz, CDC13) 5 174,72, 158,17, 82, 71,85, 44,28, 28,45.
 Clădirea 12, No.309, South 2nd Road, Zona de Dezvoltare Economică, Districtul Longquanyi, Chengdu, Sichuan, China.
Clădirea 12, No.309, South 2nd Road, Zona de Dezvoltare Economică, Districtul Longquanyi, Chengdu, Sichuan, China. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404

















.png)


